どうもこんにちは。のぶです。
今回は、はじめてコロナの話題に踏み込みたいと思います。Sobi社のアナキンラの話題です。Sobi社は、シンガポールの投資会社に買収されることが決まったようですが、一時期日本でのMSL、MAの採用活動をしていました。案内がきて、面白そうな会社だと思ったのを記憶しています。
さて、今回ですが、アナキンラの早期使用が死亡リスクを低下させるらしいので、その論文を見ていきたいと思います。
論文アブストラクト

可溶性ウロキナーゼプラスミノーゲンアクチベーター受容体(suPAR)の血清レベルの早期上昇はCOVID-19が呼吸不全に進行するリスクの増加を示している。SAVE-MORE試験(二重盲検無作為化対照試験)では、 血漿中のsuPARが6ng ml-1以上で 呼吸不全に移行するリスクがあるCOVID-19患者594名を対象に、IL-1α/β阻害剤であるanakinraの有効性と安全性を評価しました。85.9%(n=510)の患者がデキサメタゾンを投与されていました。Clinical Progression Scale(WHO-CPS)11点で評価)の調整比例オッズは、プラセボと比較してアナキンラで0.36(95%信頼区間0.26-0.50)でした。 28日目のWHO-CPSのベースラインからの低下の中央値は、プラセボ群で3ポイント、アナキンラ群で4ポイントでした。(オッズ比(OR)=0.40、P<0.0001);7日目のSequential Organ Failure Assessment(SOFA)スコアのベースラインからの低下の中央値は、それぞれ0と4であった(OR = 0.63、P = 0.004)。28日目の死亡率は低下し(ハザード比=0.45。P = 0.045)、入院期間も短くなった。
Early treatment of COVID-19 with anakinra guided by soluble urokinase plasminogen receptor plasma levels: a double-blind, randomized controlled phase 3 trial
https://www.nature.com/articles/s41591-021-01499-z.pdf
上記をまとめると…
ちょっとわかりにくいので、まとめてみます。
まず、SAVE-MOREは、Giamarellos-Bourboulis教授が独自に実施した医師主導試験Hellenic Institute for the Study of Sepsisが規制当局のスポンサー。ソビ社は、本試験に治験薬と資金を提供しているようです。
有効性
- SAVE-MORE試験の28日目の結果では、ICU(集中治療室)退室までの平均時間が4日短縮、 さらに重症呼吸不全への進行を3倍近く抑制する効果が認められました。
- アナキンラの投与により、完全に回復する可能性がプラセボおよびSOCを投与された患者に比べて2.8倍高くなりました。
- SRF(Severe respiratory failure)に移行する可能性のあるCOVIDの重症肺炎患者のうち、SOC(Standard of Care;標準治療)とアナキンラを併用した患者とSOCとプラセボを併用した患者では、28日目の時点で全体の臨床状態が有意に改善しました(オッズ比0.36、p<0.0001)。
- 同じグループのアナキンラ治療を受けた患者では、SRFに進行した患者や死亡した患者の数が減少し(オッズ比0.46、p<0.01)、COVID-19感染の証拠がない状態で退院した患者の数も増加した(オッズ比0.36、p<0.0001)。
- 28日死亡率は、SoCおよびアナキンラ治療に割り付けられた患者で55%低下した。
安全性
- SAVE-MORE試験では、アナキンラとSOC(標準治療)を併用した患者では、SOCのみを投与した患者に比べて、重篤な治療上の有害事象(TEAE)の発生率が低かった。
- 重篤ではないTEAE(治療関連有害事象)の発生率は、両投与群で同程度
サマリー
- SAVE-MORE試験はCOVID-19が進行する恐れのある患者を対象にした初めての大規模かつ無作為化対照試験であり、疾患の進行を防ぎ、死亡リスクを低減するためには、anakinraによる早期介入が有効であることを実証しています。
薬剤・結果の特徴は?1つ目の特徴
SAVE-MOREは、SRFのリスクがあるCOVID-19患者を対象に、病状の進行や死亡を防ぎ、病状の回復を促進することを目的として、ICU入室前に評価をした初めての試験だそうです。
本試験では、中等度または重度の肺炎患者を対象とし、血漿中のバイオマーカーであり予後判定ツールでもあるsuPAR(soluble urokinase plasminogen activator receptor)の上昇を測定することで、SRFのリスクがある患者を特定しました。このバイオマーカーは、初期の免疫活性化を反映し、様々な疾患において予後不良と関連することが知られています。
併用された治療法は、デキサメタゾン、抗凝固剤、レムデシビルなどで、両群間で類似していました。
ということで、COVID-19の標準治療がSOCが、日本だと厚労省の出している以下の指針が参考になりそうです。
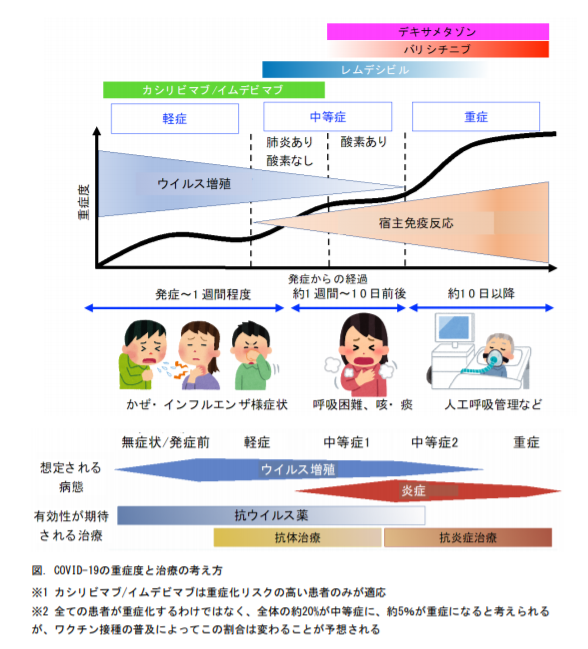
COVID-19 に対する薬物治療の考え方 第 8 版 (2021年7月31日 )
https://www.kansensho.or.jp/uploads/files/topics/2019ncov/covid19_drug_210731.pdf
日本のガイドラインには抗凝固薬は入っておりませんが、論文中には、標準治療について記載がありました。以下参考までに載せます。
All patients were receiving pre-defined standard of care, which consisted of regular monitoring of physical signs, oximetry and anti-coagulation.
論文:Early treatment of COVID-19 with anakinra guided by soluble urokinase plasminogen receptor plasma levels: a double-blind, randomized controlled phase 3 trial
つまり、すべての患者は、あらかじめ決められた標準治療を受けていて、その内容は身体的徴候の定期的なモニタリング、酸素濃度の測定、抗凝固剤の投与などで構成されていました。ということで、海外では抗凝固薬が標準なのでしょう。
2つ目の特徴は?
COVID-19感染に対する過剰な炎症反応は、疾患の進行や死亡の主要な原因となっており、この過剰な炎症を標的とし、その進展を防ぐことができる薬剤が緊急に必要とされています。それで、今回、早期治療によって重症化のリスクを低減できることがSAVE MORE試験で示すことができたということです。
COVID-19感染症は、感染者の炎症反応の過剰反応(「サイトカインストーム」と呼ばれる)により、重症化して死に至ることがありますが、アナキンラは、COVID-19による炎症亢進に重要な役割を果たすサイトカインであるIL-1α/βを標的とする抗炎症薬です。疾患の早期段階でIL-1α/βをブロックすることでCOVID-19の疾患の進行を抑制することができるようです。現在までに、COVID-19の炎症反応の治療薬として承認された薬剤はないということですので、そういう意味では本剤がはじめてになるのでしょうか。
アナキンラ(製品名:キネレット)はどんな製品?

キネレット®は、インターロイキン1のα・β受容体拮抗薬で、米国では「中等度から重度の活動性を有する関節リウマチにおける症状の軽減および構造的損傷の進行の抑制」を効能・効果としています。
米国では、18歳以上で1種類以上の疾患修飾性抗リウマチ薬(DMARDs)が無効となった患者、新生児発症多系統炎症性疾患(NOMID、クリオピリン関連周期性症候群(CAPS)の一種である)、インターロイキン-1受容体拮抗薬欠損症(DIRA)の治療に用いられています。
欧州では、「成人において、メトトレキサートとの併用により、メトトレキサート単独では効果不十分な関節リウマチの症状を改善すること」を効能・効果としています。
日本では、承認されていない薬剤です。残念です。ほかの疾患領域でも承認がおりていません。
また、キネレットは、成人、青年、小児、生後8カ月以上で体重10kg以上の乳幼児を対象に、新生児発症型多系統炎症性疾患(NOMID)、慢性乳児神経・皮膚・関節症候群(CINCA)、マックルウェルズ症候群(MWS)、家族性寒冷自己炎症症候群(FCAS)などのクリオピリン関連周期性症候群(CAPS)の治療に用いられます。
キネレットは、家族性地中海熱(FMF)の治療に使用されます。キネレットは、必要に応じてコルヒチンと併用して投与されます。また、全身性若年性特発性関節炎(SJIA)、成人発症型スティル病(AOSD)を含む、体重10kg以上の成人、青年、小児、乳児で、中等度から高度の疾患活動性を有する全身症状のあるスティル病、または非ステロイド性抗炎症薬(NSAID)やグルココルチコイドによる治療後も疾患活動性が持続する患者さんの治療にも適応があります。キネレットは、単剤または他の抗炎症薬や疾患修飾性抗リウマチ薬(DMARDs)との併用で投与することができます。
suPARおよびsuPARnostic®について
suPAR (soluble urokinase plasminogen activator receptor)は、ViroGates社のsuPARnostic®製品で検出されるバイオマーカーで、血漿中のタンパク質であり、すべてのヒトで測定可能です。suPARは、心血管疾患、腎臓疾患、2型糖尿病、癌などの疾患領域において、疾患の存在、疾患の重症度および進行、臓器障害および死亡リスクを示す一般的なリスク状態のバイオマーカーと考えられています。
最後に
今回の記事では、はじめてCOVID-19を取り上げてみましたが、いかがでしたでしょうか。
専門家の先生方からは色々とご意見があろうかと思いますが、治療の選択肢が増えることが良いことだと思います。それだけ助かる可能性が上昇しますので。あとは当局がこの結果をどうとらえて承認するのかしないのか、ですかね。企業も承認を出すものとは思っていますが、どうなんでしょうか。今後に期待です。